2025年12月31日,苏州泽璟生物宣布与全球生物制药巨头艾伯维(AbbVie)就其核心在研产品ZG006(Alveltamig)达成全球战略合作与许可选择权协议。这一交易不仅刷新了近年来中国创新T细胞衔接抗体(T cell engager,TCE)分子“出海”的重要里程碑,也再次将Delta样配体蛋白3(Delta-like ligand 3,DLL3)靶点推向小细胞肺癌(Small Cell Lung Cancer, SCLC)治疗舞台的中心。

ZG006开发与商业化权益许可公告(图片来源:泽璟官网)
根据协议,艾伯维将获得ZG006在大中华区以外市场的独家开发与商业化权利,泽璟制药则保留大中华区(中国大陆及港、澳地区)全部权益。该交易首付款即达1亿美元,总潜在价值超过12亿美元。在当前全球生物医药投融资趋紧的背景下,这一合作无疑体现了跨国药企对DLL3×TCE技术路线的高度认可。
DLL3属于Notch通路(Notch 1,Notch 2,Notch 3)相关配体,在正常组织中表达极低,却在SCLC及神经内分泌瘤中高度特异性表达,长期被认为是极具潜力的治疗靶点。
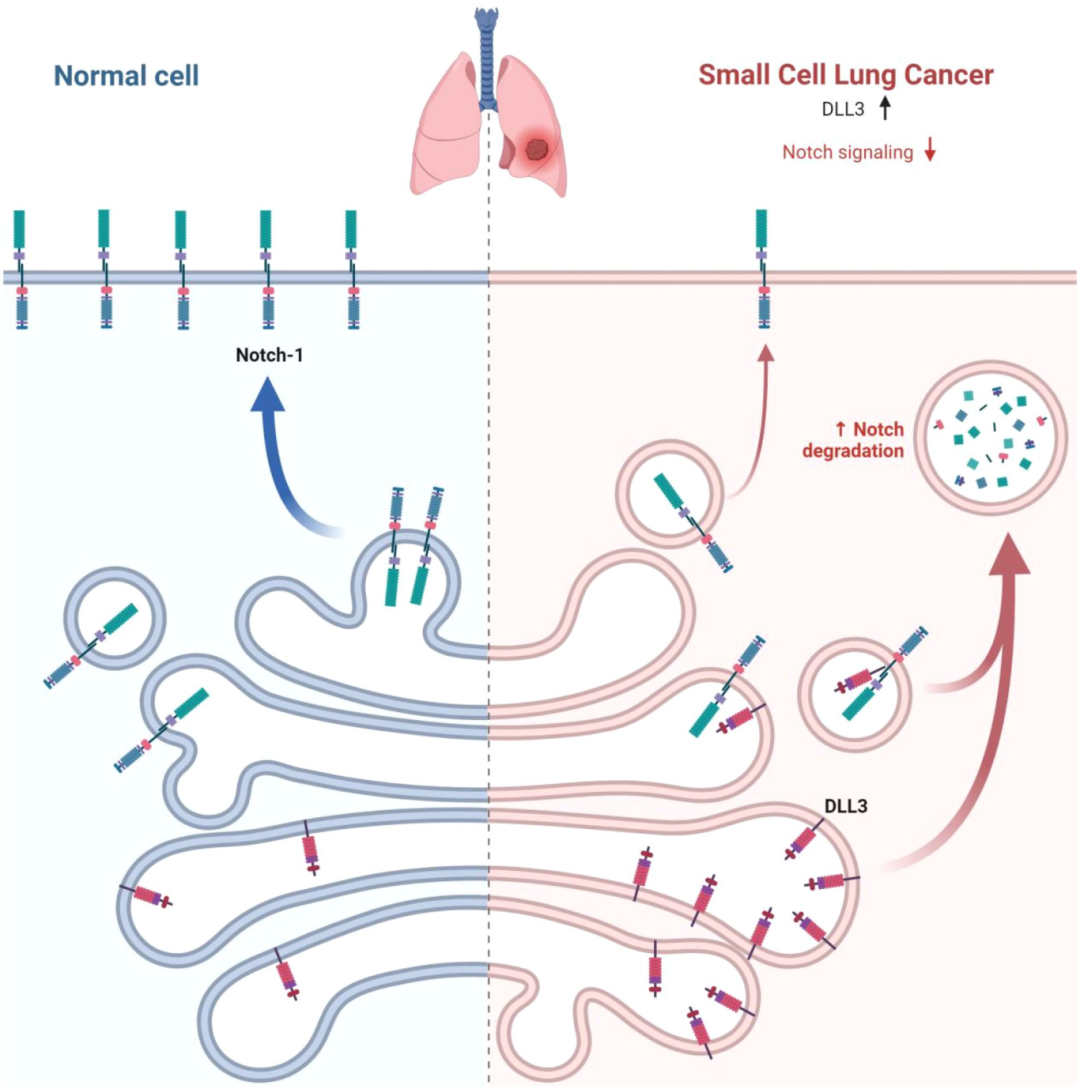
SCLC中,DLL3过表达并抑制Notch信号通路导致Notch信号失调,进而促进肿瘤发展1
艾伯维早年引进的Rova-T(DLL3-ADC)管线因临床III期失败而被迫终止,曾一度令市场对DLL3产生疑虑。但复盘来看,Rova-T的失败更主要源于 ADC技术本身的局限、毒素选择与激进的临床开发策略,而非DLL3靶点的生物学问题。近年来,随着TCE技术的成熟,DLL3重新焕发生机。无论是已获批的Tarlatamab,还是本次被艾伯维看中的ZG006(Alveltamig),均在复发/难治SCLC中展现出60–70%的最佳客观缓解率 (Objective Response Rate,ORR) ,并在无进展生存期(Progression-Free Survival,PFS)和总生存期(Overall Survival,OS)层面显示出了优于ADC的潜力。
ZG006(Alveltamig)是一种DLL3/DLL3/CD3三特异性TCE。与早期以“最大化T细胞激活”为核心目标的TCE不同,ZG006的设计理念更接近当前全球领先药企对下一代TCE的共识——在维持高效肿瘤杀伤的同时,最大限度提升安全性与治疗的可持续性。
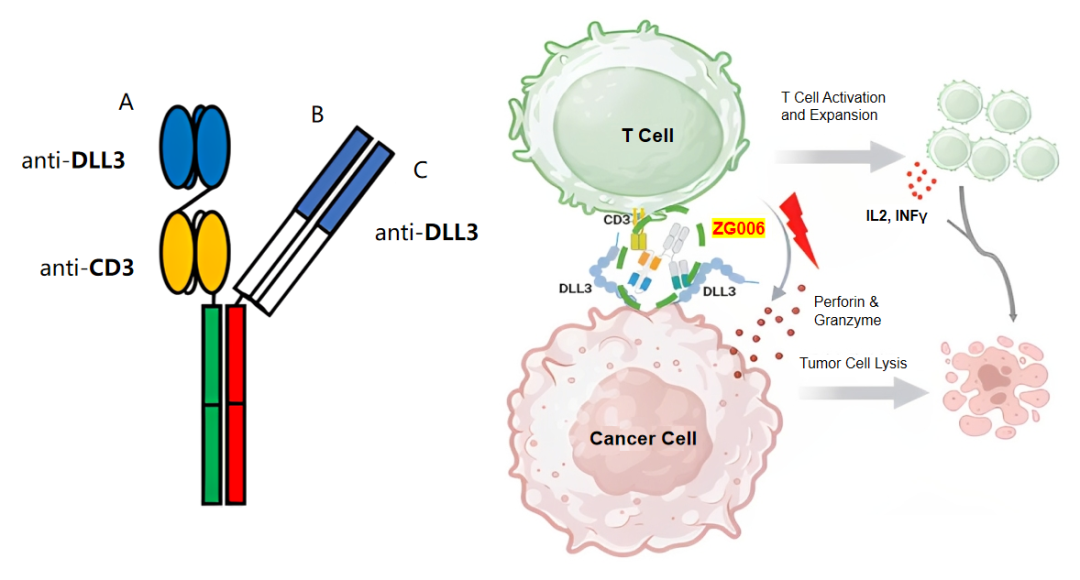
ZG006结构与作用机制(图片来源:泽璟官网)
在分子工程层面,ZG006通过多重结构创新实现了这一目标:
👉 双DLL3结合臂设计:同时针对DLL3上两个不同位点形成协同效应,显著增强对DLL3的总体结合能力。
👉 两种经生化验证的结合模式:可在单一DLL3分子上实现双位点高亲和力结合,亦可与同一肿瘤细胞表面的两个DLL3分子产生潜在的“交联”效应,强化对肿瘤细胞的接触与稳定黏附。
👉 弱化CD3结合亲和力:在保证T细胞有效募集与激活的前提下,降低非特异性T细胞活化风险,从源头改善细胞因子释放综合征(Cytokine Release Syndrome,CRS)等安全性问题;
👉 效应因子弱化的Fc区设计:以半衰期延长和系统暴露提升为主要功能,而非介导额外免疫效应,从而进一步提升可控性。
这一系列精细化设计,使ZG006即便在DLL3表达水平较低的肿瘤微环境中仍可维持稳定、持续的免疫突触形成,为T细胞杀伤提供坚实的结构基础。
2025年ESMO-Asia,泽璟生物公布了II期剂量优化研究数据(ZG006-002)。结果表明,ZG006在三线及以上SCLC患者中展现出令人瞩目的疗效与安全性平衡。
有效性方面(IRC评估):在10mg和30mg两个剂量组中,
-
疾病控制率(Disease Control Rate,DCR):均为73.3%;
-
中位PFS:7.03个月 vs 5.59个月;
-
6个月持续缓解(6-month Duration of Response rate,DoR)率:71.8% vs 69.5%;
-
12个月OS:69.1% vs 58.2%。
安全性方面:
-
ZG006-002未发生因治疗相关不良事件(Treatment-Related Adverse Event,TRAE)导致的永久停药;
-
最常见的TRAE为CRS及发热等不良事件,发生级别多为1–2级,时间集中于早期周期且能够快速缓解。
更值得关注的是,相较Tarlatamab,ZG006在T细胞活性持续性、细胞因子分泌及T细胞耗竭控制方面显示出更优趋势,为其长期疗效提供了生物学依据。
高品质工具加速SCLC生物药研发进程
目前,靶向DLL3已成为SCLC治疗的热点,药物研发主要集中在ADC及BiTE/TCE抗体。其中,BiTE抗体塔拉妥单抗(Tarlatamab)已于2024年5月获FDA加速批准,用于铂类化疗后进展的广泛期SCLC(ES-SCLC)患者。“为更好生物医药”,ACROBiosystems百普赛斯推出包括DLL3及Notch 1、2、3在内的多个SCLC热门分子高品质药物开发工具,全面满足小细胞肺癌生物药开发需求。
🪄重组蛋白:DLL3、Notch 1、Notch 2、Notch 3,均由人源细胞表达,覆盖多物种、多标签,经SEC-MALS、ELISA、SPR及BLI验证,具有高纯度、高活性、高批间一致性的特点,适用于免疫、抗体筛选、候选药物功能验证等应用。

🪄 DLL3过表达细胞株 (HEK293、CHO):DLL3抗原在宿主细胞膜表面进行长期稳定表达,可全面满足早期药物发现与筛选、研究接近天然表达水平目标蛋白功能等应用场景。

🪄 另有多种SCLC相关生物药开发靶点工具可选,全面满足您的SCLC药物开发需求。
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-
DLL3蛋白:经SDS-PAGE验证>95%,SEC-MALS验证>95%,具备高纯度
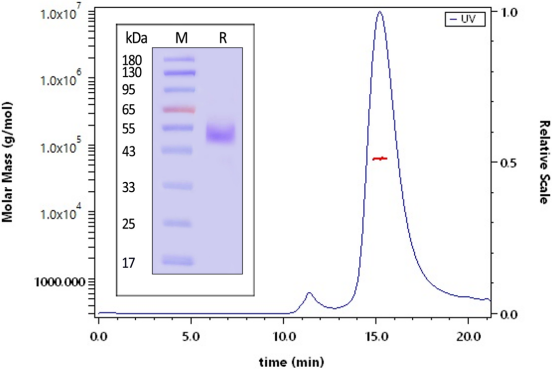
The purity of Human DLL3 Protein, His Tag (MALS verified) (Cat. No. DL3-H52H4) is greater than 95% verified by SDS-PAGE and more than 95% verified by SEC-MALS.
-
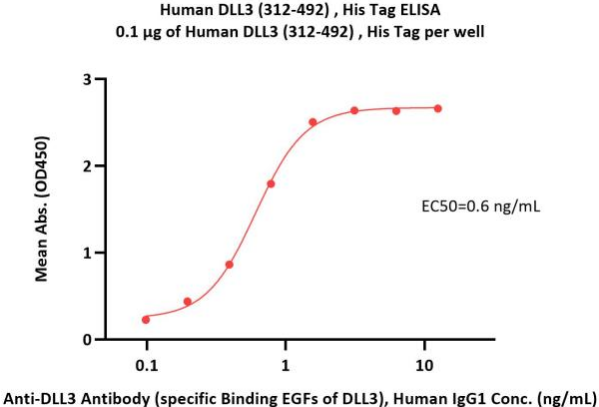
DLL3蛋白:经ELISA验证,具备高生物活性
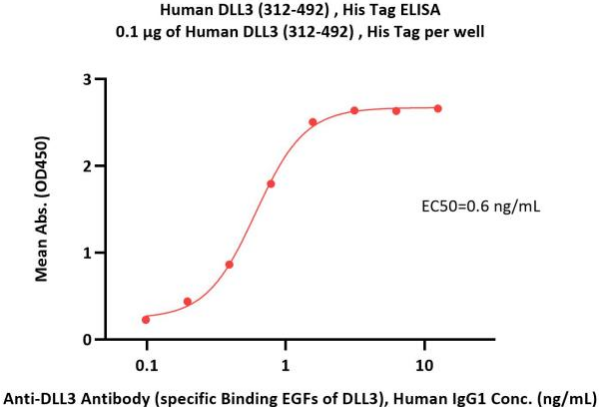
Immobilized Human DLL3 (312-492), His Tag (Cat. No. DL3-H52Hz) at 1 μg/mL (100 μL/well) can bind Anti-DLL3 Antibody (specific Binding EGFs of DLL3), Human IgG1 with a linear range of 0.1-2 ng/mL (QC tested).

-
Notch 1蛋白:经SPR验证,具备高亲和力
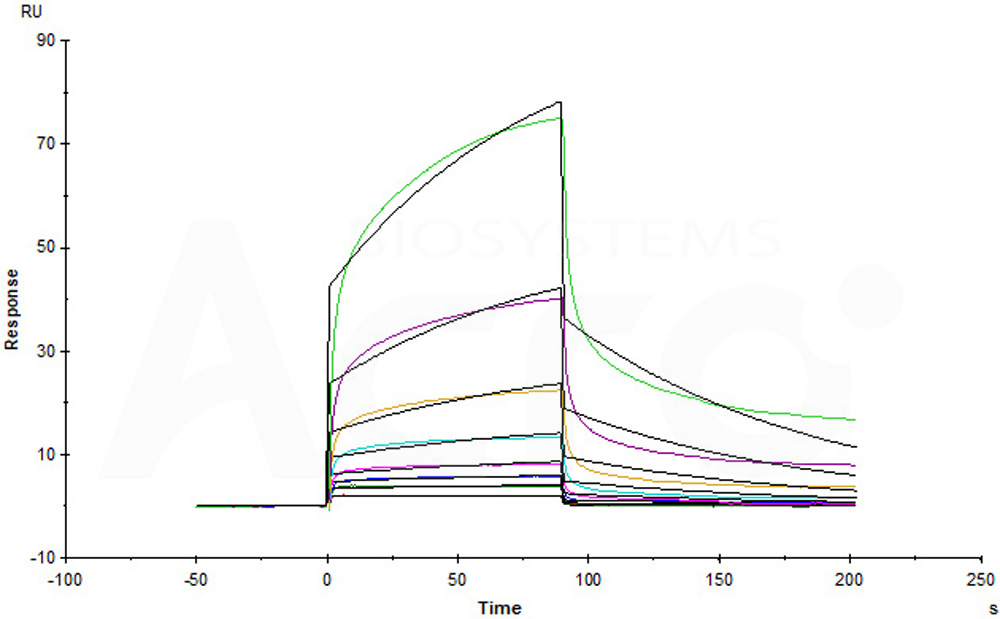
Human Jagged 1, His Tag (Cat. No. JA1-H52H9) immobilized on CM5 Chip can bind Human NOTCH1, Fc Tag (Cat. No. NO1-H5255) with an affinity constant of 5.13 μM as determined in a SPR assay (Biacore T200) (Routinely tested).

-
DLL3过表达细胞株:经FACS验证,确保DLL3稳定表达
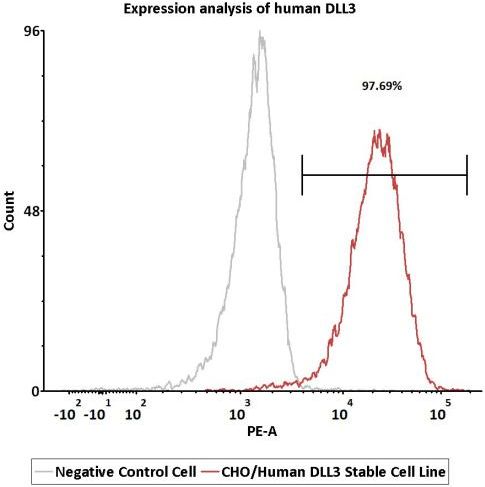
Cell surface staining was performed on CHO/Human DLL3 Stable Cell Line (Cat. No. SCCHO-ATP111) or negative control cell using anti-human DLL3 antibody followed by staining with PE anti-human IgG Fc Antibody.

更多双抗及ADC药物开发工具推荐

>>点击图片了解双抗药物开发工具
参考资料:
1. Ding J, Yeong C. Advances in DLL3-targeted therapies for small cell lung cancer: challenges, opportunities, and future directions. Front Oncol. 2024 Dec 5;14:1504139. doi: 10.3389/fonc.2024.1504139. PMID: 39703856; PMCID: PMC11655346.

ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)